Edutorial - Medische hulpmiddelen
Hier kunt u edutorials (informatie met uitleg) vinden over medische hulpmiddelen. DARE!! laat graag zien, doormiddel van deze edutorials, hoe bepaalde onderwerpen onderzocht moeten worden en hoe deze uitgevoerd kunnen worden. Heeft u vragen over dit onderwerp mail ons dan op info@dare.nl of vul het formulier in onderaan deze pagina.
Medische Hulpmiddelen en Usability
Edutorial
Usability, oftewel gebruiksvriendelijkheid, wordt een steeds belangrijker concept bij het ontwikkelen van een medisch hulpmiddel. De reden hiervoor is dat een gebruiksvriendelijk product de kans op gebruiksfouten verkleint en daarmee de veiligheid naar een hoger niveau tilt. Ook de fabrikant zelf heeft uiteraard voordeel bij een gebruiksvriendelijk product omdat dit de klanttevredenheid stimuleert, wat weer zijn weerslag heeft op de verkoop.
Gebruiksvriendelijkheid heeft voornamelijk betrekking op de gebruikersinterface, oftewel de interactie tussen gebruiker en product. Onder de gebruikersinterface vallen bijvoorbeeld knoppen, hendels, lichtjes, schermpjes, alarmsignalen, maar ook de gebruikershandleiding en eventuele veiligheidsinformatie. Het gaat in het kader van het beoordelen van gebruiksvriendelijkheid om risico's die kunnen optreden bij normaal gebruik en de daarbij te verwachten gebruiksfouten. Voorzienbaar misbruik maakt hier geen deel van uit; beoordeling hiervan hoort thuis bij risicomanagement.
De mate waarin een product ontworpen is met aandacht voor gebruiksvriendelijkheid (usability engineering), en de documentatie daarvan, wordt beoordeeld door de Notified Body in het kader van CE-markering. Uiteraard zullen de meeste engineers de gebruiksvriendelijkheid vanzelfsprekend meenemen in het ontwerpproces, op zijn minst door vast te stellen aan welke eisen de gebruikersinterface moet voldoen. Toch is het belangrijk elke stap in dit proces van het begin af aan goed te documenteren, omdat dit tijd en kosten kan besparen op een later tijdstip.
Een goede methode hiervoor is beschreven in de EN 62366. Gebruik van deze norm wordt verplicht gesteld door de norm voor productveiligheid van medische hulpmiddelen, de EN60601-1. In grote lijnen lijkt het proces zoals beschreven in de EN 62366 overeen te komen met het proces van risicomanagement zoals beschreven in de EN 14971. Het verschil is dat er in de EN 14971 sprake is van een besluitvormingsproces ter vaststelling van acceptabele risico's. Dit is terwijl de EN62366 in eerste instantie een ontwerp- en ontwikkelingproces weergeeft van de gebruikersinterface. Hierdoor is ook het risico's gerelateerd aan gebruiksvriendelijkheid meegenomen. Wel kunnen deze risico's weer gebruikt worden als input voor het proces van risicomanagement volgens de EN 14971.
De mate van uitgebreidheid van het proces, van usability engineering en eventuele bijbehorende testen, zal passend moeten zijn bij de risicoklasse en het type product. Daarnaast zal ook de complexiteit van het gebruik en het beoogde doel van het product bij de risicolasse moeten worden opgenomen.
Usability engineering
Het hele proces begint met het goed definiëren van het product. Dit begint met vaststellen wie het product gaat gebruiken. Belangrijk hierbij is de vraag of het gaat om een zorgprofessional (denk bijvoorbeeld aan een ECG monitor) of juist om de patiënt die ongetraind is, bijvoorbeeld bij een elektrische rolstoel. Ook de personen die andere handelingen uitvoeren met het product, zoals schoonmaken of installeren, zijn in dit kader gebruikers. Daarnaast dient vastgesteld te worden hoe het product gebruikt gaat worden, of het werkingsprincipe en de omgeving van gebruik. Tenslotte dient vastgesteld te worden waarvoor het product zal worden gebruikt. Kortom wat de medische indicatie is die door het product wordt verholpen, vastgesteld of verlicht.
Deze kennis kan verzameld worden op basis van onderzoek onder gebruikers. Hierbij kan gedacht worden aan het verzamelen van informatie over gebruikers. Daarnaast kan ook het observeren van gebruikers met vergelijkbare producten in de dagelijkse omgeving en een sessie met een klein groepje typische gebruikers. Of tevens een formeel onderzoek volgens een protocol waarin een steekproef van gebruikers typische taken uitvoert in een echte of gesimuleerde omgeving.
Op basis van bovenstaande gegevens kan dan worden vastgesteld aan welke eisen de gebruikersinterface moet voldoen. Hierbij moet worden vastgesteld welke functies bij het dagelijks gebruik vaak gebruikt zullen worden (en daardoor een grotere kans geven op ontstaan van gebruiksfouten) en welke functies direct gerelateerd zijn aan veiligheid (bijvoorbeeld aan een functie om het alarm uit te schakelen). Deze functies gezamenlijk de belangrijkste gebruiksfuncties vormen. In het uiteindelijke ontwerp zullen deze functies voor de gebruiker makkelijk te herkennen moeten zijn.
Een ander belangrijk aspect bij het vaststellen van de eisen aan de gebruikersinterface is het definiëren van de verschillende gebruiksscenario's en ook van eventuele 'worst case' scenario's. Hierbij dient ook gedacht te worden aan gebruiksscenario's in het kader van onderhoud, reiniging, vervoer of opslag en de gebruiksfouten die hieruit kunnen ontstaan (verkeerd hanteren), welke weer kunnen leiden tot schade aan het product.
Tevens dient bepaald te worden welke risico's ten aanzien van de gebruikersinterface naar voren komen bij bepaalde ontwerpkeuzes en hoe deze afgevangen kunnen worden door het ontwerp aan te passen. Deze risicoanalyse, die overigens in een later stadium tijdens en na het vaststellen van het ontwerp. Deze moet daarna bij elke ontwerpwijziging opnieuw uitgevoerd worden. Dit komt in feite overeen met een risicoanalyse in het kader van risicomanagement. Bij het bepalen van de risico's dient men een aantal zaken te overwegen. Voorbeelden hiervan zijn, de omgeving waarin het product gebruikt zal gaan worden, taakgerelateerde eisen, bijvoorbeeld goed schoon te maken, draagbaar, met een hand te bedienen, typische gebruiksscenario's en de te verwachten gebruiksfouten. Het gaat hierom fouten die kunnen ontstaan doordat de gebruiker de werking van het product verkeerd begrijpt of doordat het juiste gebruik tegen intuïtief is en onduidelijkheden in de gebruikershandleiding.
Tenslotte is het noodzakelijk te onderzoeken welke risico's gerelateerd aan gebruiksvriendelijkheid er bekend zijn aan de hand van vergelijkbare producten of eerdere generaties van het product. Ook dient de state-of-the-art van de huidige techniek in acht genomen te worden.
De eisen die gesteld worden aan de gebruikersinterface moeten zo zijn gekozen dat risico's als gevolg van normaal gebruik en gebruiksfouten zoveel mogelijk worden uitgesloten of verminderd. In het beginstadium zullen de eisen van algemenere aard zijn, maar naarmate de ideeën voor het ontwerp vastere vorm gaan aannemen, worden deze specifieker. Van belang is dat de eisen zo meetbaar mogelijk gesteld worden. Uiteindelijk zullen de eisen worden vormgegeven als kwantificeerbare technische specificaties.
Uiteindelijk kan de ontwerpfase starten, waarin de gebruikersinterface wordt ontworpen volgens de vastgestelde eisen. Specifiekere aanwijzingen ten aanzien van ontwerpkeuzes op het gebied van gebruiksvriendelijkheid zijn te vinden in ANSI/AAMI HE75:2009, een uitgebreide technische handleiding op dit gebied. Ook in de EN 60601-1 serie zijn er verschillende subnormen die meer specifieke eisen stellen, bijvoorbeeld aan alarmen of symbolen op toetsen. Reeds tijdens de ontwerpfase kan het aan te raden zijn testen over gebruiksvriendelijkheid met gebruikers uit te voeren, bijvoorbeeld door middel van ontwerpmodellen of prototypes.
Verificatie en validatie van het ontwerp
Om zeker te zijn dat het uiteindelijke ontwerp goed is, moet het geverifieerd en gevalideerd worden. Verificatie dient om vast te stellen dat het uiteindelijke ontwerp inderdaad voldoet aan de gestelde eisen, terwijl validatie breder is en dient om vast te stellen dat het ontwerp voldoet aan de behoeften van de gebruiker en aan het beoogde doel. Ter bevordering van de objectiviteit dient de validatie uitgevoerd te worden door een persoon die niet direct bij de ontwerpfase betrokken is geweest. De validatie gaat over alle soorten van interactie tussen product en gebruiker, dus bijvoorbeeld ook onderhoud en reiniging. Validatie kan uitgevoerd worden door testen met betrekking op de gebruiksvriendelijkheid. Hierbij een steekproef van gebruikers het product gebruikt in een gesimuleerde omgeving (wat nabootsing van worst-case scenario's mogelijk maakt) of in de werkelijke omgeving. Deze gebruikers beoordelen dan relevante aspecten van het product zoals gemak van gebruik, werkdruk, snelheid, tevredenheid met het product, duidelijkheid van de instructies enzovoorts. Tevens kunnen er veldtesten plaatsvinden in de werkelijke klinische omgeving.
Tenslotte zal er opnieuw een risicoanalyse proces moeten plaatsvinden op het uiteindelijke ontwerp. Als er nog risico's blijken te zijn die niet door een aanpassing in het ontwerp afgevangen kunnen worden, moeten de gezondheidsvoordelen opwegen tegen deze risico's.
Samenvattend is het dus van groot belang om het hele proces van usability engineering van het begin af aan gedegen uit te voeren en goed te documenteren. Benodigde aanpassingen in het ontwerp die pas ontdekt worden als de productiefase van start gaat, kosten veel meer tijd en geld om op te lossen dan wanneer dat in een vroeger stadium gedaan was. Het opzetten en uitvoeren van gedegen usability engineering zorgt ervoor dat de kans dat er tijdens de laatste validatie vlak voor productie nog fouten naar voren. Hierdoor kunnen fouten in het algemeen aanzienlijk worden verminderd.

Certificatie van een medisch elektronisch product: een praktische aanpak
Elk medisch hulpmiddel dat op de markt gebracht wordt, moet voldoen aan de Medische Hulpmiddelen Richtlijn of, als het een actief (elektronisch) implantaat betreft, aan de Richtlijn actieve implanteerbaar medische hulpmiddelen. Deze edutorial beschrijft het certificatieproces voor een medisch elektronisch hulpmiddel (in de richtlijn een actief hulpmiddel genoemd) welke onder de Europese Richtlijn Medische Hulpmiddelen valt.
De weg naar certificatie
Een product wordt als medisch hulpmiddel gezien als het door de fabrikant bestemd is om bij de mens te worden gebruikt om ziektes of handicaps op te sporen, te behandelen, of te verlichten of om ziektes te voorkomen. Om te bepalen welke stappen er genomen moeten worden, is het van belang eerst de klasse te bepalen. Afhankelijk van de klasse en in hoeverre u als fabrikant een kwaliteitssysteem heeft, kan vervolgens bepaald worden welke route naar conformiteit gekozen moet worden. Tenslotte is het van belang dat alle vereiste documentatie up-to-date is. Het proces van het opstellen van documentatie begint uiteraard al vanaf het allereerste stadium, en het is van belang in dat stadium al rekening te houden met de vereisten voor certificatie, om te zorgen dat er geen onnodige vertragingen optreden om het product op de markt te krijgen. Deze edutorial zal de bovengenoemde stappen die genomen moeten worden op de weg naar certificatie in meer detail toelichten.
Classificatie en conformiteit
De klasse van een medisch hulpmiddel is afhankelijk van de risico's die het met zich meebrengt. Als voorbeeld in duur en plaats van toepassing (hulpmiddelen in contact met het zenuwstelsel worden bijvoorbeeld hoger geclassificeerd dan die in contact met de huid). Daarnaast zijn er een aantal specifieke regels voor de actieve medische hulpmiddelen, echter bij het toepassen van deze regels moeten ook de algemene regels niet vergeten worden. Op de website van de Europese Commissie is een toelichtend document te vinden (MEDDEV 2.4/1 rev.9) welke aan de hand van flowcharts en voorbeelden heel duidelijk laat zien hoe een hulpmiddel geclassificeerd moet worden.
Klasse I hulpmiddelen zijn de hulpmiddelen met het laagste risico. Hierop is in principe zelfcertificatie van toepassing; dat houdt in dat u als fabrikant uw technische documentatie opstelt, waarmee u, indien door de autoriteiten verzocht, kunt aantonen dat het product veilig is en aan de essentiële eisen uit de richtlijn voldoet. Het is dan niet nodig om een Notified Body in te schakelen. Echter, wanneer het hulpmiddel een meetfunctie heeft of steriel geleverd wordt, moet dit aspect wel door een Notified Body beoordeeld worden. Houdt er rekening mee dat, ook al betreft het zelfcertificatie, het wel een verplichting is om aan alle eisen voor wat betreft de technische documentatie te voldoen (er moet bijvoorbeeld ook een klinische evaluatie verricht worden).
Klasse IIa en IIb hulpmiddelen zijn risicovoller, en daarom is het noodzakelijk een Notified Body in te schakelen om de producten en/of uw kwaliteitssysteem te laten beoordelen. Klasse-III producten komen onder de elektronische hulpmiddelen niet voor (tenzij het actieve implantaten betreft, maar die vallen onder een andere richtlijn).

Als fabrikant kunt u er zelf voor kiezen of u uw producten, of uw kwaliteitssysteem, of een combinatie wilt laten certificeren. Dit hangt ervan af of u een kwaliteitssysteem volgens EN 13485 heeft, en zo ja, of u daarbij controle heeft over zowel design als productie of alleen productie. Ook de klasse van het hulpmiddel speelt een rol. Als u in het geheel geen kwaliteitssysteem heeft, dan kunt u ervoor kiezen om alle geproduceerde hulpmiddelen te laten verifiëren door een Notified Body. Uiteraard is dit alleen een optie als het een beperkte oplage betreft. In de meeste gevallen heeft de fabrikant echter minimaal een productie kwaliteitssysteem in huis, welke u dan kunt laten certificeren door een Notified Body. Betreft het een klasse IIb hulpmiddel, dan zult u daarnaast ook het ontwerp moeten laten checken door middel van een typekeur, bij dezelfde of bij een andere Notified Body. Als u zowel het ontwerp als de productie onder controle heeft met uw kwaliteitssysteem, kunt u deze laten certificeren en is er geen typekeur meer nodig. In alle gevallen wordt uw technisch dossier, naast eventueel het kwaliteitssysteem, beoordeeld door de Notified Body; bij een typekeur voor elk type product, en bij een kwaliteitssysteem certificatie op basis van monstername.
Productveiligheid onderzoek en testen volgens de EN 60601-1
In alle gevallen, ook bij klasse I producten, dient aangetoond te zijn dat het product veilig is en de essentiële werkzaamheid gegarandeerd blijft. Hiertoe zal het product ontworpen en getest moeten worden volgens de EN 60601-1. Strikt genomen is het nooit verplicht om normen te gebruiken, echter normen geven wel een 'vermoeden van overeenstemming' met de richtlijn. Mocht u de norm niet gebruiken, zult u op een andere manier moeten aantonen dat het product voldoet aan de essentiële eisen, en dat is een lastige zaak. EN 60601 onderzoek en testen kunt u laten uitvoeren bij een geaccrediteerd testlaboratorium.
Op dit moment is de derde editie van de EN 60601-1 van kracht (EN 60601-1:2006). Ook amendement A1 hiervan is inmiddels geharmoniseerd. Hoewel er een overgangstermijn is, is het verstandig om nieuwe producten gelijk volgens dit amendement te laten testen. Tegelijk is in sommige gevallen ook nog de tweede editie van de EN 60601-1 van kracht, namelijk als er sprake is van een geharmoniseerde subnorm die nog naar deze editie verwijst. Het is dus belangrijk om van te voren, eventueel in overleg met het testlaboratorium, vast te stellen welke versie van de norm en welke subnormen van toepassing zijn.
Subnormen kunnen zowel horizontale als specifieke productnormen betreffen. Een voorbeeld van horizontale normen waarmee vaak rekening gehouden moet worden zijn bijvoorbeeld de EN 60601-1-8 over alarmen en EN 60601-1-11 over thuisgebruik (incl. thuizorg) van medische hulpmiddelen. Specifieke productnormen omvatten bijvoorbeeld normen over holters, pulseoximeters etc.
Naast de subnormen worden er nog een aantal andere normen verplicht gesteld door de EN 60601-1; de meest belangrijke hiervan zijn de EN 14971 over risicomanagement en de EN 62366 over usability. Omdat beide normen verplicht zijn om te kunnen voldoen aan de EN 60601-1, zal het testlaboratorium hier ook al (grotendeels) naar kijken.
In het geval van risicomanagement stelt de EN 60601-1 de aanwezigheid van een risicomanagement proces verplicht volgens de EN 14971. Alleen de eisen met betrekking tot verzamelen van post-productie informatie en bijhouden van de risico analyse naar aanleiding hiervan is voor de EN 60601-1 niet verplicht. Hier zal het testlaboratorium dus niet naar kijken. Risico analyse hangt samen met de clausules van de EN 60601-1 en kan daar verschillende rollen in spelen. Als een bepaalde clausule uit de EN 60601-1 aangeeft aan welke eisen het betreffende aspect van het hulpmiddel moet voldoen en daarbij acceptatiecriteria aangeeft, dan kan in de risicoanalyse geconcludeerd worden dat het risico van dat spect acceptabel is, als het hulpmiddel deze criteria haalt. In sommige clausules zijn echter geen acceptatiecriteria aangegeven, deze dienen dan bepaald te worden door middel van een risicoanalyse. Tenslotte zijn er nog clausules die alleen specifieke gevaren benoemen, waarbij in de risicoanalyse moet worden vastgesteld wat de eisen zijn aan de testen en wat de acceptatiecriteria zijn. Ook moet in de risicoanalyse worden vastgesteld of er nog sprake is van andere gevaren die niet aan de orde gekomen zijn in de EN 60601-1.
Een belangrijk onderdeel in dit proces is het vaststellen van de 'essential performance'. Hierbij moet eerst worden vastgesteld wat de performance in normale conditie is. Vervolgens dient gekeken te worden welke mogelijke degradatie van deze performance op kan treden in foutconditie en dient het risico hiervan bepaald te worden. Als een bepaalde mate of vorm van degradatie een onacceptabel risico geeft, dan kan daarmee bepaald worden wat de essential performance is om vrij te blijven van dat onacceptabele risico. Deze essential performance dient gehandhaafd te worden tijdens de testen uit de EN 60601-1, en ook dienen risico maatregelen genomen te worden om te zorgen dat deze essential performance ook in foutcondities gehandhaafd blijft. De essential performance kan ook een volledig verlies van functie inhouden, als dit bijvoorbeeld herkenbaar is voor de gebruiker en geen gevaar oplevert, of als er maar geen verkeerde signalen of ongewenste output geleverd wordt. Een essential performance kan bijvoorbeeld gedefinieerd worden als het in werking treden van een alarm bij verlies van functie.
Risicomanagement volgens de Richtlijn
De eisen die de EN 60601-1 stelt aan risicomanagement zijn beperkter dan die waaraan volgens de richtlijn moet worden voldaan. Ten eerste sluit de EN 60601-1 eisen aan het bijhouden van de risicoanalyse binnen post-productie uit. Om te voldoen aan de eisen uit de richtlijn, dient er ook een plan aanwezig te zijn voor het continu bijhouden van deze informatie en verwerken daarvan in het risicomanagementproces. Nadat het hulpmiddel op de markt is gebracht, dient informatie uit de markt aantoonbaar verzamelt en verwerkt te worden. Ten tweede kijkt de EN 60601-1 specifiek naar risico's die direct samenhangen met het product, terwijl het voor een volledige, betrouwbare risicoanalyse en risico/voordeel afweging ook van belang is te kijken naar specifieke klinische risico's, bijvoorbeeld als gevolg van de medische handeling die eventueel samenhangt met het gebruik van het hulpmiddel, eventuele bijwerkingen etc.
Het belangrijkste verschil tussen de EN 14971 en de richtlijn gaat over de inschatting van risico's als acceptabel of niet. De EN 14971 stelt simpelweg dat het aan de fabrikant is om vast te stellen welke risico al dan niet acceptabel wordt geacht, en stelt dat gestopt mag worden met risicoreductie als een acceptabel niveau is bereikt.

Ook mogen economische afwegingen hierin meegenomen worden. De richtlijn stelt echter dat risico's zo ver als mogelijk moeten worden gereduceerd, tot het niveau waarop verdere vermindering niet mogelijk is of geen extra veiligheidsvoordeel oplevert. Pas daarna mag worden vastgesteld of de risico's acceptabel zijn. Economische overwegingen mogen hierin in principe geen rol spelen. Alle risico's die niet gereduceerd kunnen worden tot een acceptabel niveau moeten worden afgewogen, apart en gezamenlijk, tegen het medische voordeel. Uiteraard is het erg lastig in te schatten wanneer een risico nu voldoende is gereduceerd met deze aanpak. Daarom heeft de Notified Body Recommendation Group (NBRG) een toelichtend document opgesteld om de zaak te verhelderen. " Consensus Paper for the Interpretation and Application of Annexes Z in EN ISO/IEC 14971: 2012".
Houdt er rekening mee dat dit nog wel een draft betreft. Het NBRG advies voor het zover als mogelijk reduceren van risico behelst in grote lijnen het volgende: indien bij bepaalde risico's gebruik is gemaakt van methoden en eindpunten uit geharmoniseerde normen, waarbij het risico gereduceerd is tot dit eindpunt, mag dit risico als acceptabel worden beschouwd. Dit is in lijn met bijvoorbeeld de EN 60601-1, die specifiek stelt dat risico's acceptabel worden geacht als de eisen en acceptatiecriteria uit de norm behaald zijn. Als er geen geharmoniseerde normen zijn, kan worden teruggegrepen op andere erkende normen. Als er helemaal geen normen zijn, dan zal de fabrikant een afweging moeten maken tegen de state-of-the-art, aan de hand van informatie uit de klinische praktijk, medische literatuur, vigilante databases etc. Als het betreffende aspect voldoet aan de state-of-the-art dan mag het risico in principe als acceptabel worden geacht. Tenslotte, voor die risico's die niet aan bovengenoemde voldoen, maar waarbij verdere reductie niet meer bijdraagt aan de veiligheid, zal een risico/voordeel analyse moeten plaatsvinden. Belangrijk is om niet te vergeten om ook voor alle gecombineerde restrisico's samen een dergelijke afweging te maken.
Technische documentatie
Voor elk medische hulpmiddel dat op de markt gebracht gaat worden, dient er een technische documentatie te zijn. Deze technische documentatie moet in ieder geval de gegevens bevatten zoals hieronder aangegeven.
1. Beschrijving product
- Identificatie van het product
- Werkingsmechanisme en specificaties
- Prestaties van het product
- Beoogd gebruik
- Beoogde gebruikers en omgeving van gebruik
- Medische indicatie
- Beschrijving van eventuele productvarianten en beoogde combinaties
- Classificatie met toelichting
- Een 'draft' verklaring van overeenstemming
2. Lijst toegepaste normen
Er dient een overzicht aanwezig te zijn van (geharmoniseerde) normen welke eventueel zijn toegepast.
3. Ontwerp en constructie
- Overzicht van relevante essentiële eisen uit annex I van de richtlijn welke van toepassing zijn op het product. Wanneer bepaalde eisen niet relevant geacht worden, dient een toelichting aanwezig te zijn.
- Technische beschrijving van het product: ontwerpschema's, print lay-outs, stuklijsten, overzicht veiligheid kritische componenten incl. uitleg en datasheets.
- Een omschrijving van software en de verificatie en validatie daarvan.
- Testrapporten.
- Handleiding en etikettering.
4. Preklinische evaluatie
- Een overzicht van gebruikte materialen die in contact komen met patiënt of gebruiker dient aanwezig te zijn.
- Evaluatie van biocompatibiliteit dient aanwezig te zijn, in principe volgens EN 10993. Indien geen testen zijn uitgevoerd op dit gebied (bijvoorbeeld omdat het materiaal al een lange geschiedenis van probleemloos gebruik kent), dient dit besluit goed onderbouwd te zijn. Dan dient ook onderbouwd te zijn hoe gegarandeerd is dat het precies hetzelfde materiaal en dezelfde productieprocessen betreft.
- Wanneer proefdieronderzoek verricht is, dient een beschrijving aanwezig te zijn van het uitgevoerde onderzoek, incl. doelstellingen, methodologie, rationale voor keuze van proefdiersoort, analyse en resultaten.
- Benchtesten / simulatietesten dienen, indien verricht, beschreven te zijn.
5. Klinische evaluatie
Wanneer er reeds eerder onderzoek is verricht met een product met een equivalente technologische werking en een equivalente medische indicatie kan een literatuuronderzoek voldoende zijn. Wanneer het gaat om een nieuwe technologie, een nieuwe medische indicatie of als er aanleiding is ontstaan uit de risicoanalyse. Bijvoorbeeld indien er een groot risico is verwacht of de risico / voordeel verhouding kan niet afdoende worden ingeschat zal er een klinisch onderzoek verricht moeten worden. Deze moeten aansluiten op de aspecten die niet met het literatuuronderzoek konden worden afgedekt.
Aspecten die beoordeeld dienen te worden door middel van de klinische evaluatie hebben betrekking op de klinische werkzaamheid, klinische veiligheid, adequaatheid van de gebruiksinstructies en etikettering en risico's ten opzichte van voordelen.
Meer informatie over het opzetten en documenteren van een klinische evaluatie is te vinden in MEDDEV 2.7/1 rev.3 Clinical evaluation: Guide for manufacturers and notified bodies.
Ten aanzien van literatuuronderzoek dienen de volgende gegevens in een getekend en gedateerd rapport aanwezig te zijn:
- Beschrijving methodologie literatuuronderzoek (doelstellingen, databronnen, zoekstrategie, onderbouwing dat alle relevante positieve en negatieve publicaties meegenomen zijn, exclusiecriteria).
- Onderbouwing dat het product uit de literatuur equivalent is aan het huidige product (ten aanzien van beoogd gebruik, klinische eigenschappen, biocompatibiliteit, technische kenmerken).
- Een weging van individuele referenties (afhankelijk van robuustheid onderzoeksmethode, expertise auteur etc.).
- Analyse (beoogde werkzaamheid aangetoond, evt. risico's en veiligheidsmaatregelen voortkomend uit de evaluatie, afweging risico's / voordelen).
Het kan aan te raden zijn om het klinisch onderzoeksprotocol bij wijze van pre-check ter beoordeling voor te leggen bij een Notified Body, zodat alvast duidelijk kan worden of het protocol op zich wel of niet acceptabel is (dit geeft uiteraard nog geen garanties over de uiteindelijke conclusie). Een Notified Body mag geen advies geven, dus zal dan alleen een beoordeling kunnen uitvoeren.
6. Usability
Usability, ofwel gebruikersvriendelijkheid, is een belangrijk aspect bij een medisch hulpmiddel. Het is reeds in de ontwerpfase van belang om rekening te houden met gebruikersvriendelijkheid en dit ook te documenteren.
Samengevat zijn er drie belangrijke aspecten waaraan voldaan moet worden:
- vaststellen van gevaren die kunnen ontstaan tijdens normaal gebruik en gebruiksfouten en het verkleinen hiervan door risico verlagende maatregelen;
- verificatie van vooraf gestelde eisen aan de gebruikersinterface;
- validatie door middel van vooraf gestelde criteria.

De geanalyseerde risico's worden gebruikt als input voor de verificatie en validatie eisen. Vervolgens dienen de risico's verkleint te worden op dezelfde wijze als bij risicomanagement, waarna het aangepaste ontwerp opnieuw beoordeeld wordt ten aanzien van eventuele nieuwe risico's en opnieuw geverifieerd en gevalideerd wordt.
Verificatie en validatie maken dus een belangrijk onderdeel uit van usability engineering. Het verschil tussen beide is als volgt: verificatie dient om vast te stellen dat de gebruikersinterface voldoet aan vooraf vastgestelde, meetbare eisen of specificaties (een voorbeeld van een dergelijke eis: een knop voor een bepaalde functie moet een bepaalde afmeting hebben en zich op een bepaalde plaats bevinden). Het vaststellen van deze eisen maakt onderdeel uit van het usability proces en moet dus ook terug te vinden zijn in de usability file. Validatie is breder, en maakt gebruik van representatieve gebruikers om vast te stellen dat het ontwerp functioneert zoals zou moeten in het 'dagelijks gebruik'. Criteria om dit vast te stellen nemen bijvoorbeeld de volgende vorm aan. 'een bepaald percentage van de representatieve gebruikers moet in staat zijn deze bepaalde handeling met het device in een aantal minuten foutloos uit te voeren'.
Het vaststellen van de risico's, eisen, criteria voor validatie en verificatie zijn gericht op de gebruikersinterface, ofwel meer specifiek:
- veelgebruikte functies van het product;
- functies die direct gerelateerd zijn aan veiligheid (denk b.v. aan alarmfuncties).
Deze dienen omschreven te zijn in de usability file.
De volgende informatie is vereist ten behoeve van het vaststellen van risico's, en dient dus in de usability file aanwezig te zijn:
- specificatie van toepassing (indicatie, gebruikersprofiel, wijze van gebruik etc.);
- taakgerelateerde eisen (welke eisen er gesteld worden aan het apparaat om zijn taak uit te kunnen voeren);
- typische gebruikersscenario's (incl. worst case scenario's);
- gebruiksfouten, denk hierbij ook aan gebruiksfouten die ontstaan doordat de gebruiker een verkeerd begrip zou kunnen hebben van de werkzaamheid van het device.
De uiteindelijk vastgestelde risico's (inclusief de methoden om ze te verkleinen en de controle daarop) kunnen meegenomen worden als onderdeel van de risicoanalyse, maar er dient dan wel een verwijzing opgenomen te zijn in de usability file en het dient duidelijk te zijn welke risico's gerelateerd zijn aan usability.
Ten behoeve van verificatie van de gebruikersinterface, dienen er meetbare eisen te zijn vastgesteld om de usability van de veelgebruikte functies en de veiligheidsfuncties vast te kunnen stellen, inclusief eisen om vast te stellen of deze functies afdoende herkenbaar zijn voor de gebruiker (in de norm wordt dit programma van eisen de usability specification genoemd). De input voor deze eisen is de informatie die gebruikt is om de risico's vast te stellen, inclusief de risico's zelf.
Ten behoeve van validatie dient er een validatieplan te zijn, gebaseerd op de vastgestelde typische en worst-case gebruiksscenario's. Deze beschrijft de methode en criteria op basis waarvan de validatie wordt uitgevoerd en op welke wijze representatieve gebruikers onderdeel hiervan zijn.
Alle onderdelen van het gebruik moeten steeds meegenomen worden, dus niet alleen het klinische gebruik, transport, opslag, installatie en afvoe/verwijdering (en dus ook, naast gebruikers, b.v. servicepersoneel). Indien een van deze onderdelen niet van toepassing is omdat de fabrikant deze handeling zelf verricht (b.v. installatie), dient dit toegelicht te worden in de usability file. Ook de handleiding en overige informatie maken onderdeel uit van het usability proces.

Tenslotte zijn er nog enkele belangrijke punten over de gebruikershandleiding en eventuele training:
- De handleiding dient het werkingsprincipe, fysische en performance eigenschappen, medische indicatie en toepassingsgebied, beoogde patiëntenpopulatie en het gebruikersprofiel te omvatten.
- Als training noodzakelijk wordt geacht door u als fabrikant, dient informatie aanwezig te zijn over de vereiste duur en frequentie van training en wie deze uit gaat voeren (vereiste competentie).
Wanneer er userinterfaces van een andere fabrikant gebruikt worden, denk hierbij b.v. aan het operating systeem op een computer of een besturing van een onderdeel van het medische apparaat, moeten deze interfaces ook meegenomen worden in de usability file. Deze interfaces worden ook wel “Userinterface of unknown provenance” of wel “UOUP” genoemd.
Als leidraad kan de EN-IEC 62366-1 gebruikt worden. Daarnaast is dan ook de EN-IEC 60601-1-6 van toepassing. Deze laatste norm legt in feite de link tussen de EN-IEC 62366-1 en de EN-IEC 60601-1.
7. Risicoanalyse
Bij een risicoanalyse wordt, naast normaal gebruik, ook voorzienbaar misbruik meegenomen in de analyse. In de technische documentatie dient een risicomanagementplan aanwezig te zijn. Ook risicomanagement is een doorlopend proces, waarbij informatie uit de markt na het productiestadium als input gebruikt wordt in het risicomanagementproces.
De volgende punten moeten aanwezig zijn in de risicomanagement file zijn:
- Bewijs van kwalificatie van het personeel dat de risicoanalyse heeft uitgevoerd.
- Beschrijving van redelijkerwijs voorzienbaar misbruik.
- Een overzicht van kwalitatieve en/of kwantitatieve eigenschappen van het hulpmiddel die gerelateerd zijn aan veiligheid en het garanderen van 'essential performance'.
- Identificatie en beschrijving van bekende en voorzienbare gevaren die kunnen ontstaan door een opeenvolging van gebeurtenissen / handelingen met het product.
- Inschatting van de risico's verbonden met deze gevaren en criteria voor acceptabel risico (ernst afgewogen tegen kans van optreden van schade).
- Wijze van risicobeheersing, waarbij risico's zo ver als mogelijk verkleint dienen te worden, in eerste instantie door het ontwerp inherent veilig te maken. Als dat niet mogelijk is kan er teruggegrepen worden op inherente veiligheidsmechanismen zoals alarmen. Tenslotte, als dit ook niet mogelijk blijkt of afdoende is, dienen instructie en waarschuwingen opgenomen te worden voor de restrisico's.
- Van risico's die niet tot een acceptabel niveau kunnen worden teruggebracht (uitgaand van normen of state-of-the-art) dient een afweging gemaakt te worden of de voordelen opwegen tegen de risico's. Hiertoe dient een overzicht aanwezig te zijn van de ingeschatte gevaren, de geassocieerde risico's en een risico / klinisch voordeel afweging (acceptabel, niet acceptabel of alleen acceptabel in specifieke omstandigheden).
- Als eindanalyse dient ook de combinatie van alle restrisico's afgewogen te zijn tegen het klinische voordeel.
- Veiligheid is meestal conditioneel; condities voor veiligheid dienen aangegeven te zijn (dit hangt o.a. samen met de risicoanalyse en het beoogde gebruik; bijvoorbeeld de conditie dat het hulpmiddel alleen door getraind personeel gebruikt mag worden).
- Informatie voor de gebruiker ten aanzien van veiligheid, voortkomend uit de risicoanalyse, dient duidelijk aanwezig te zijn in de gebruikershandleiding en/of de etikettering.
- Een beschrijving is aanwezig van maatregelen (ontwerp, productie en verpakking) die genomen zijn om te garanderen dat het product optimaal blijft functioneren gedurende de levensduur van het product.
- Een omschrijving van een strategie om te verzekeren dat gebruikerservaring verzameld wordt, evenals informatie uit publicaties van het product of vergelijkbare producten. Deze informatie dient vervolgens als input gebruikt te worden in het risicomanagementproces.
8. Post market surveillance
In de technische documentatie dient een plan aanwezig te zijn welke de strategie ten aanzien van post market surveillance omschrijft. Er dient omschreven te worden hoe de informatie van gebruikers en patiënten verzameld wordt. De mate van diepte van de surveillance is afhankelijk van de ingeschatte risico's. In het plan moet ook zijn aangegeven hoe eventuele verbeteringen aan het product die voortkomen uit de ervaringen uit de markt worden doorgevoerd.
In een aantal gevallen dient de post market surveillance ook een plan voor post market klinische follow-up te omvatten (zie MEDDEV 2.12/2 rev.2 Post Market Clinical Follow-up studies). In de volgende gevallen kan dit aan de orde zijn:
- Het gaat om een innovatief product, technologie, materiaal of om een nieuwe medische indicatie.
- Producten met een hoog risico of voor doelgroepen met een hoog risico.
- Indien veiligheid en werkzaamheid op lange termijn niet zeker is.
- Bijwerkingen etc. die gebleken zijn uit de klinische evaluatie of uit eerdere post-market surveillance.
- Toepassing in doelgroepen die niet meegenomen zijn in de eerdere klinische evaluatie en waarbij een andere risico / voordelen afweging verwacht wordt.
- Als er grote discrepantie is tussen de verwachte levensduur van het product en redelijke tijdsduur van pre-market klinisch onderzoek.
- Risico's die bekend zijn van vergelijkbare producten.
- Indien niet zeker is of veiligheid en werkzaamheid hetzelfde zullen zijn in een meer gevarieerde groep van gebruikers.
Daar waar de CE-markering gebaseerd is op equivalentie in plaats van op een eigen onderzoek.
Afwezigheid van een PMCF dient in voldoende mate onderbouwd te worden.

Classificatie medische hulpmiddelen
Voordat een medisch hulpmiddel op de markt kan worden gebracht, moet eerst vastgesteld zijn dat het veilig is in gebruik en de geclaimde werkzaamheid behaald wordt. Voor laag-risico hulpmiddelen mag de fabrikant dit zelf doen door middel van zelfcertificatie tegen de Richtlijn Medische hulpmiddelen. Bij hogere klassen is een aangewezen instantie (Notified Body) nodig om het hulpmiddel goed te keuren. Onlangs is DARE!! Certifications geaccrediteerd voor de stap voorafgaand hieraan: het certificeren van elektronische medische hulpmiddelen. Dit artikel licht iets over dit onderwerp toe.
Voor medische hulpmiddelen zijn veel ontwikkelingen gaande. Aan de ene kant vinden er continu innovaties plaats, gebaseerd op de nieuwste technieken. Bijvoorbeeld voor telemedicine, wat zorg op afstand in de vergrijzende maatschappij haalbaar maakt, of combinaties tussen medische hulpmiddelen en mobiele apps. Dit zorgt voor een naadloze aansluiten bij de kritische, zelfstandige patiënt die geen tijd en zin heeft in regelmatige ziekenhuisbezoeken. Aan de andere kant zie je een doorlopende tendens naar steeds strengere regelgeving. Immers al die nieuwe innovaties brengen allemaal weer eigen risico's met zich mee, waar de fabrikant, de zorgverlener en de certificerende instelling goed op in moeten springen.
Al enige tijd is DARE!! zich aan het oriënteren op de mogelijkheden om zelf een certificerende instelling te worden. Gezien onze lange ervaring met productveiligheidsonderzoeken en EMC-testen op elektronische medische hulpmiddelen, ook wel actieve medische hulpmiddelen genoemd, was het een passende volgende stap. Dit is ook om de certificering van medische hulpmiddelen op ons te nemen. Wij spelen hiermee in op de vraag van onze klanten, die graag het complete traject (testen én certificeren) door ons zouden willen laten uitvoeren. Daarom zijn we al sinds 2010 bezig om geaccrediteerd te worden voor het certificeren van medische hulpmiddelen. Kortgeleden is de accreditatie uiteindelijk rond gekomen en vanaf nu kunnen we dus actieve medische hulpmiddelen certificeren. Dit kan gedaan worden volgens de annex III (typekeur) en annex IV (eindproductverificatie) van de Richtlijn Medische hulpmiddelen. Met een certificaat van DARE!! kunt u naar een Notified Body toe, die het product op basis van ons certificaat zal goedkeuren. De volgende stap die DARE!! zal nemen, is aanwijzing aanvragen bij het VWS, zodat DARE!! als Notified Body het product ook de finale goedkeuring kunnen geven. Tenslotte zullen we onze activiteiten op termijn uitbreiden naar het certificeren van uw kwaliteitssysteem, zodat we het hele plaatje kunnen bieden.
Afhankelijk van de classificatie van uw medisch hulpmiddel, zijn er verschillende wegen te bewandelen om een certificaat te verkrijgen. Onderstaand schema geen een overzicht hiervan. DARE!! is op dit moment geaccrediteerd voor de geel gemarkeerde blokken.
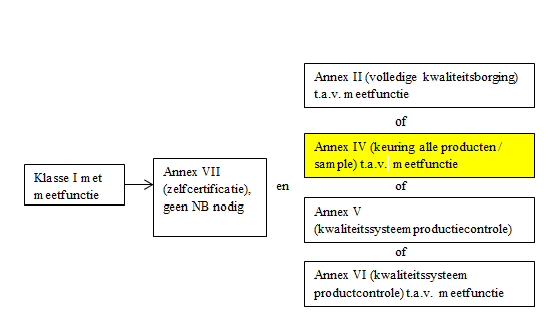
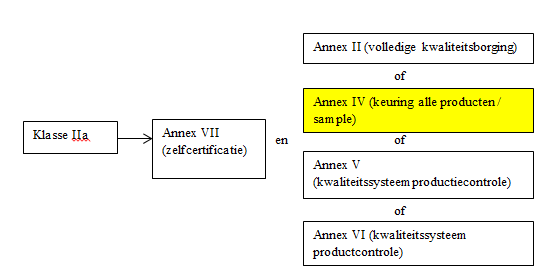
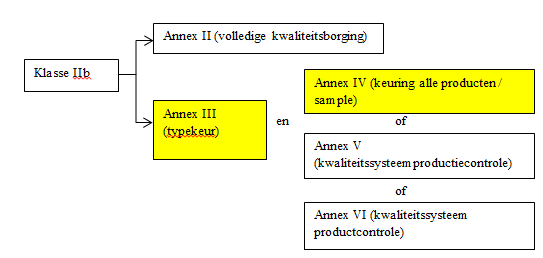
Een belangrijk onderdeel van certificatie, en daar wijkt dit proces af van productveiligheidsonderzoek, is dat niet alleen de veiligheid gecontroleerd moet worden, maar ook de geclaimde performance. Tegelijkertijd zien we bij productveiligheidsdonderzoek en EMC al de tendens dat veel subnormen steeds meer performance claims in zich opnemen, waarbij de geclaimde performance het uitgangspunt is voor het slagen of falen voor een test. Het afwegen van performance is bij DARE!! dus regelmatig al onderdeel van productveiligheidsonderzoek. Bij certificatie gaat dit nog een stap verder, en dient ook gekeken te worden naar de preklinische en klinische evaluaties die de fabrikant verricht heeft om de performance van zijn product vast te stellen. Bij een certificatie traject wordt er dus veel diepgaander naar het product en vooral ook de toepassing van het product gekeken. Regelmatig zullen we hierbij de hulp in roepen van klinische experts in het veld, die immers de meest uitgebreide en recente kennis op hun vakgebied hebben. DARE!! onderhoudt hiertoe nauwe banden met verschillende academische ziekenhuizen.
Tevens zult u ons regelmatig aan kunnen treffen op de verschillende beurzen en conferenties over medische hulpmiddelen. Zo hebben we begin juni een stand gehad op een van de grootste medische hulpmiddelen beurzen in Europa, de MEDTEC, in Stuttgart, en zijn we dit najaar aanwezig op het Technology voor Health event in Den Bosch. Mocht u vragen hebben over het certificeren van uw medisch hulpmiddel, kunt u ons op een van de beurzen aanschieten, of uiteraard direct contact opnemen.